砷对人体的危害之大,是众所周知的,砷中毒就是过量摄入砷化物,导致身体多系统发生中毒的现象。
砷中毒的机理是砷离子与体内蛋白质中的羟基(-OH)、巯基(-SH)结合,使蛋白酶失去活性,导致细胞不能正常呼吸和代谢,引起中毒反应。
砒霜就是砷化物的一种,主要成分为三氧化二砷。

工业上,有多个领域的烟气中含砷量较高,比如:铜冶炼厂烟气、黄磷尾气、煤矸石砖厂烟气等。富砷烟气不但加速了高温烟气对金属基体的腐蚀,同时对中低温烟气的防腐涂层也提出了新的挑战。
志盛威华集团生产的一系列高、中、低烟气防腐涂料,针对腐蚀介质中砷的作用,对涂料成膜物质专门做了的氟的封端和加密,目前可以做到在含砷烟气中至少5年内不会被破坏失效!
这一系列防腐涂料有:ZS-1034耐酸碱防腐涂料(耐温300℃)、ZS-711无机防腐涂料(耐温400℃)、ZS-1041烟气防腐涂料(耐温600℃)、ZS-811耐高温防腐涂料(800℃)、ZS-1021高温封闭涂料(1200℃)、ZS-822复合陶瓷高温防腐涂料(耐温1400℃)等。

砷的出现使本来不用做防腐的钢材很快就烂个底掉,同时让原本能防护好的涂层破坏掉,这不得不让厂家重新考虑防腐材料的选择。
那么,砷的危害和破坏性为什么如此厉害呢?有兴趣的朋友请跟着艾工一起来了解一下这个奥秘吧!
下面是学习时刻:
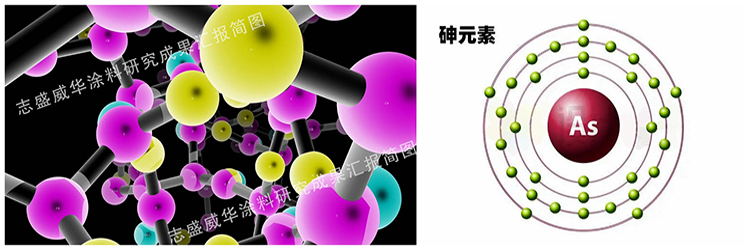
砷的元素符号为As,俗称砒,是第33号元素,属于类金属元素,偏金属性,但有时也会表现出非金属性,其价态通常有+3、+5、-3,但在某些特殊情况下,也可以是其他化合价,比如在二硫化二砷(As2S2)中,砷元素的化合价为+2价。
砷原子核外有33个不同运动状态的电子,其核外电子排布为:1S22S22P63S23P64S23d104S24P3,即有18个轨道。可以看出,其最外面有3个孤对电子,次外层有1对成对电子。
因此砷既可以失去3个电子表现出金属性,也可以得到3个电子表现出非金属性,同时它还可以失去5个电子(最外面3个孤对电子和次外层1对电子)表现出金属性。甚至在一些特殊条件下,它可以得到或失去任意数量的电子,与其它元素形成配位络合物。
这就是砷的厉害之处,同为第5主族元素,氮和磷也有类似性质,但是砷的原子质量更大,原子半径也更大,因此砷的这种性质达到了极致。至于锑和铋,主要就是金属性了,其非金属性在大多时候都非常不明显了。
砷化物的常见形式有二硫化二砷(As2S2)、三硫化二砷(As2S3)、三氧化二砷(As2O3)、五氧化二砷(As2O5)、砷化等。
钢铁等金属表面为了平衡其表面活性,通常会吸附结合环境中的巯基(-SH)、羟基(-OH)、羰基(C=O)、碳酰基(=CO)等官能团。
砷化物,尤其是+3价砷和-3价砷常常诱导产生活性氧、活性硫等自由基,造成氧化应激,从而与钢铁表面的官能团结合,破坏了金属表面的化学平衡,使金属原子重新处于裸露状态,重新表现出极大的金属活性,从而使本来已经钝化的金属表面周而复始地循环被腐蚀。
同时砷化物还能让极性较强的非金属性介质(F、Cl、O、S)轻易获得电子而发生腐蚀现象。甚至,防腐涂层外层端基如果足够的惰性,稍有得到电子或者失去电子的意愿,也会被砷抓住破绽,逐个击破,一层层的破坏。
所以说,砷化物虽然在很多时候不是直接参与腐蚀反应的物质,而是金属腐蚀过程中强烈的诱导催化剂,但其作用要远远高于直接腐蚀介质,常常使腐蚀反应速率提高几十倍甚至上百倍。
